Seguridad biológica de los agentes blanqueadores dentales (I)
SEGURIDAD BIOLÓGICA DE LOS AGENTES BLANQUEADORES DENTALES (I):
Llena Puy MC 1, Amengual Lorenzo J 2, Forner Navarro L 3.
1.- Médico Adjunto del Servicio Valenciano de Salud. Profesor Asociado. Unidad Docente de Patología y Terapéutica Dentales. Departamento de Estomatología. Facultad de Medicina y Odontología.Universitat de València. Estudi General.
2.- Co-Director del Diploma en Técnicas de Blanqueamiento Dental. Universitat de València. Estudi General.
3.- Profesor Titular. Unidad Docente de Patología y Terapéutica Dentales. Departamento de Estomatología. Facultad de Medicina y Odontología. Universitat de València. Estudi General.
RESUMEN:
En este serie de revisiones, analizaremos los efectos sobre los tejidos orales de los agentes blanqueadores, así como sus efectos sistémicos potenciales.
Comenzaremos ésta serie de revisiones abordando el problema de la sensibilidad dentinaria que, en ocasiones, se asocia con los tratamientos blanqueadores y/o con las soluciones que los productos blanqueadores presentan para el tratamiento de las discoloraciones dentarias.
PALABRAS CLAVE:
Sensibilidad dentinaria, blanqueamiento dental.
1.- SENSIBILIDAD DENTINARIA:
El inconveniente que más frecuentemente se plantea en el blanqueamiento de dientes vitales es la hiperestesia dentinaria, tanto en el tratamiento domiciliario como en el realizado en la consulta dental; de tal forma que, aunque en muy pocas ocasiones, puede llegar a ser motivo de suspensión del tratamiento blanqueador.
Según la teoría de Brännström, esta hiperestesia vendría provocada por diferentes estímulos de carácter externo (como los osmóticos; los de naturaleza química; los de tipo mecánico; y los térmicos) (1-2), que originarían una aumento de la presión de fluidos en los túbulos dentinarios, provocando la hiperestimulación de las terminaciones sensitivas pulpares, lo que se traduce en dolor (2-3).
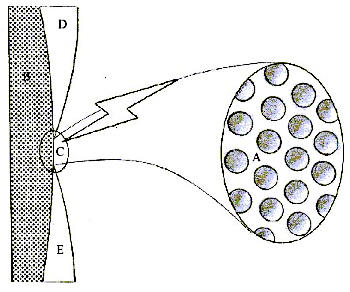
Dicha hiperestesia se produce especialmente en las primeras fases del tratamiento, debido, por un lado, a que en ocasiones la unión esmalte-cemento no es perfecta y quedan áreas de dentina expuesta a nivel del cuello dentario (4-7) (Figura 1); y por otro, al efecto de "grabado ácido" que produce el peróxido de hidrógeno sobre el esmalte que aumenta su permeabilidad y permite la difusión del peróxido de hidrógeno a su través gracias a su bajo peso molecular (8-10). Éste efecto es totalmente reversible; tras la utilización controlada en la consulta dental durante más de 100 años de peróxido de hidrógeno y de carbamida a diferentes concentraciones en el tratamiento de las discoloraciones dentarias, no se han descrito casos de necrosis pulpar atribuibles a dichos agentes blanqueadores (11-14).
|
Fig 1: Túbulos dentinarios (A); dentina (B); unión amelocementaria con dentina expuesta (C); Esmalte (D); Cemento (E). |
Las alternativas que la industria propone para reducir este efecto deletéreo que, aunque reversible como ya se ha comentado, es molesto y puede ser incluso motivo de suspensión del tratamiento son variadas; por una parte aumentar el pH de las fórmulas y por otro incorporar sustancias que tengan un efecto desensibilizante como son el flúor y el nitrato potásico. Con respecto al pH de las fórmulas, hay que señalar que en los procesos de disociación del peróxido de hidrógeno se van a producir radicales libres que en las primeras fases van a reducir el pH (15), el cual se va a recuperar transcurridos unos 15 a 20 minutos, llegando a sus valores iniciales transcurrida aproximadamente una hora (16).
El efecto de los mencionados agentes desensibilizantes es doble, por una parte los fluoruros actúan obliterando los prismas del esmalte y reduciendo el paso de sustancias a su través, mientras que el nitrato potásico incrementa el umbral de excitación de las terminaciones sensitivas pulpares (17).
Hoy por hoy, un elevado número de productos blanqueadores para uso domiciliario, incorporan agentes desensibilizantes; sin ánimo de ser exhautivos, vamos a presentar la composición de algunos de estos productos en lo que a su mecanismo desensibilizante se refiere.
Incorporan desensibilizantes:
1. FKD ( Laboratorios Kin): Peróxido de Hidrógeno al 3,5 % + nitrato potásico al 5%
2. Illuminé Home (Dentsply DeTrey): Peróxido de Carbamida al 10 y al 15 % + fluoruro sódico al 0,22%
3. Opalescence F (Ultradent): Péroxido de Carbamida al 15 y al 20 % + fluoruro sódico
4. Opalescence PF (Ultradent): Peróxido de Carbamida al 15 y al 20 % + fluoruro sódico + nitrato potásico
5. Pola Day (Southern Dental Industries Limited): Peróxido de hidrógeno al 3 y al 7,5 % + fluoruro sódioc + nitrato potásico
6. Pola Night (Southern Dental Industries Limited): Peróxido de Carbamida al 10, 16 y 22 % + fluoruro sódico + nitrato potásico
7. Pola Office (Southern Dental Industries Limited): peróxido de hidrógeno al 35 % incorpora también nitrato potásico, es el único para aplicación en clínica que lo incorpora hoy por hoy. 8. Rembrandt XTRA Comfort (Den-Mat): Peróxido de Carbamida 10 % + desensibiliante
Alcalinizan el pH:
1. Star Brite (Spectrun Dental Inc.): Peróxido de Hidrógeno al 35%
2. Contrast p.m. (Spectrun Dental Inc.): Peróxido de Carbamida al 10 y 15 %
3. Contrast p.m. plus (Spectrun Dental Inc.): Peróxido de Carbamida al 10, 15 y 20%
4. Perfecta (Premier American Dental Higienics): Peróxido de Hidrógeno (al 3 y al 4.5%) y de Carbamida (al 11, 13, 16 y 21%) a diferentes concentraciones con glicol.
BIBLIOGRAFÍA:
1. Ten AR. Estructura de los tejidos bucales. En: Histología Oral (2ª Ed). Buenos Aires: Editorial Medica Panamericana.1991. p. 65-79.
2. Martínez P, Gil FJ. Eficacia de un colutorio de nitrato potásico y fluoruro sódico en el tratamiento de la hipersensibilidad dentinaria. Periodoncia 1995; 5: 93-99.
3. Matas F, Quinteros A, Mendieta C. Hipersensibilidad dentinaria. Etiología, diagnóstico y tratamiento. Periodoncia 1997; 7: 181-92.
4. Figún ME, Garino RR. En: Anatomía Odontológica (2ª Ed). Buenos Aires: Editorial El Ateneo. 1988.
5. Ten Cate AR: En: Histología Oral (2ª Ed). Buenos Aires: Editorial Medica Panamericana.1991.
6. Silva L, Fraga JM, Santana U, Guitian F. Ultraestructura de los tajidos duros del diente. Comparación de dientes definitivos y temporales. Arch Odontoestom 1994: 10: 16-27.
7. Amengual J, Llena MC, Forner L. Morfometría de la región cervical en dientes anteriores. Arch Odontoestom 1999; 15: 407-13.
8. Arwill T, et al. Penetration of radiactive isotopes through the enamel and dentin. II. Transfer of 22-Na infresh and chemically treated dental tissues. Odontol Rev; 1999; 20: 47-52.
9. Heymann HO. Nonrestorative treatment of discolored teeth. Reports from an international symposium. J Am Dent Assoc ( suplement) 1997; 128: Introduction.
10. Dale BG, Aschheim KW. Blanqueadores y agentes relacionados. En: Odontología Estética (2ª Ed). Madrid: Ediciones Harcourt S.A. 2002. pp. 247-267
11. Haywood VB, Heymann HO. Nigthguard vital bleaching. Quintessence Int 1989; 20: 173-176.
12. Haywood VB, Heymann HO. Nigthguard vital bleaching: How safe is it? Quintessence Int 1991; 22: 515-523.
13. Tam L. Vital tooth bleaching: review and current status. Can Dent Assoc J 1992; 58: 654-663.
14. Yarborough D. The safety and efficacy of tooth bleaching: a review of the literature 1988-1990. Compend Contin Educ Dent 1991; 12: 191-196.
15. Dillenburg AL, Conceiçao. Clareamento dental. En: Dentística Saúde e Estética. Porto Alegre: Artemed Editora. 2000. pp.227-248.
16. Amengual J, Llena MC, Forner L. Evaluación de las variaciones de ph provocadas en el medio externo por el peróxido de hidrógeno en el blanqueamiento dental interno. En prensa.
17. Tam L. Vital Effect of potassium nitrate and fluoride on carbamide peroxide bleaching. Quintessence Int 2001; 32: 760-770.